Ученые получают из клеток кожи работающие яйцеклетки и нейроны: как они это делают и зачем
В сентябре 2025 года ученые впервые смогли получить функционирующую яйцеклетку человека, используя клетку кожи.
Также из клеток кожи получают нейроны, клетки сердца, печени и других органов. Правда, для этого нужны сложные технологии, заставляющие клетку «помолодеть», то есть вернуться в незрелую форму, в которой она существовала до того, как «выбрала» специализацию и стала клеткой кожи.
Такие «омоложенные» клетки потом используют для научных исследований, а еще они могут пригодиться для лечения некоторых болезней. Разберемся, как их получают и почему ученые не могут просто взять уже готовые клетки человека.
Чем ученых не устраивают готовые незрелые клетки
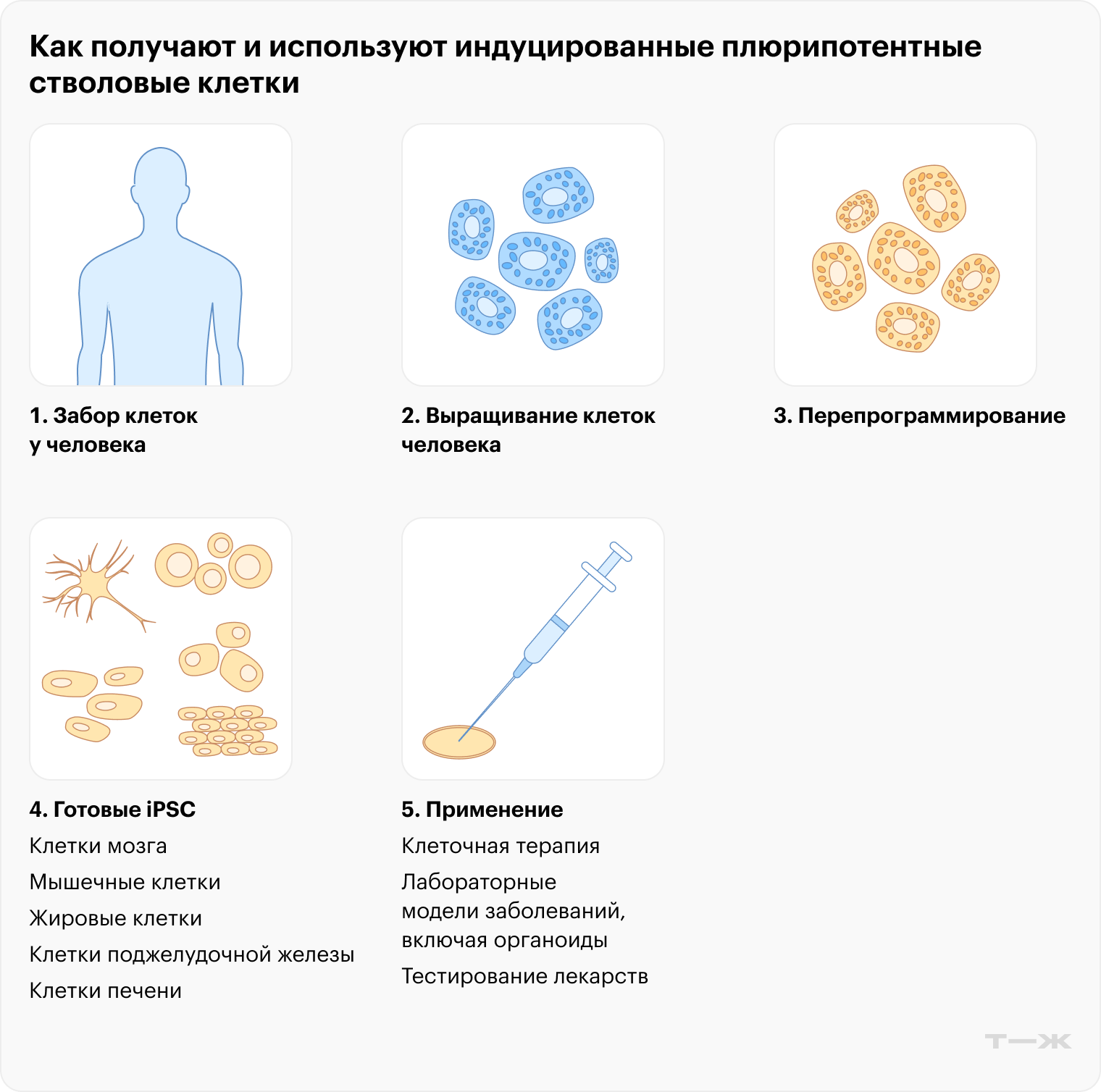
Обычно для получения новых клеток, нужных ученым, например нейронов, перепрограммируют другие зрелые клетки человека — чаще всего кожи или крови — в то, что называют iPSC, то есть индуцированными плюрипотентными стволовыми клетками (сайт недоступен из РФ). Из них можно вырастить практически любую клетку человеческого тела. Поэтому они и плюрипотентные: от латинского pluralis — множественный и potentia — возможность. По сути, это клетка со множеством возможных путей развития. А индуцированные они из-за того, что появились не сами по себе, а после действий ученых в лаборатории.
Конечно, незрелые стволовые клетки можно получать и другим путем. Например, клетки человеческих эмбрионов на самой ранней стадии развития тоже плюрипотентные — из них потом образуются все органы и ткани человеческого тела. Но использовать эмбриональный материал сложно из-за этических ограничений.
Кроме того, технология производства iPSC позволяет меньше зависеть от получения образцов. Для исследований обычно используют невостребованные или аномальные эмбрионы, оставшиеся от процедур ЭКО и переданные ученым с согласия донора, такого материала всегда не хватает.
Стволовые клетки есть и в организме взрослого человека — например, в костном мозге, коже, мышцах и некоторых других тканях. Но они способны трансформироваться только в определенные типы зрелых клеток — это нужно, чтобы восполнять специализированные клетки в конкретной ткани. Например, стволовые клетки костного мозга превращаются только в различные клетки крови. Также они делятся лишь ограниченное число раз. А эмбриональные стволовые клетки и iPSC потенциально могут размножаться бесконечно, то есть их проще выращивать в условиях лаборатории.
Как ученые получают новые клетки
Индуцированные плюрипотентные стволовые клетки в 2006 году впервые получил из фибробластов мышей японский исследователь и доктор медицины Синъя Яманака вместе с коллегами. А в 2007 году у него получилось сделать то же самое и с человеческими клетками.
Сама идея того, что зрелую клетку можно перепрограммировать, не нова: она появилась еще в середине 20 века и лежит в основе технологии клонирования организмов. При этом ядро соматической клетки , обычно той же кожи, переносят в ооцит , из которого собственное ядро удалили. С помощью специальных факторов в цитоплазме ооцит перепрограммирует свое новое ядро так, что может развиться нормальный эмбрион.
У эмбриона будут гены донора, то есть того, от кого взяли соматическую клетку. Эта технология называется SCNT — перенос ядра соматической клетки (сайт недоступен из РФ). Именно ее в 1996 году использовали для создания овечки Долли — первого клона млекопитающего.
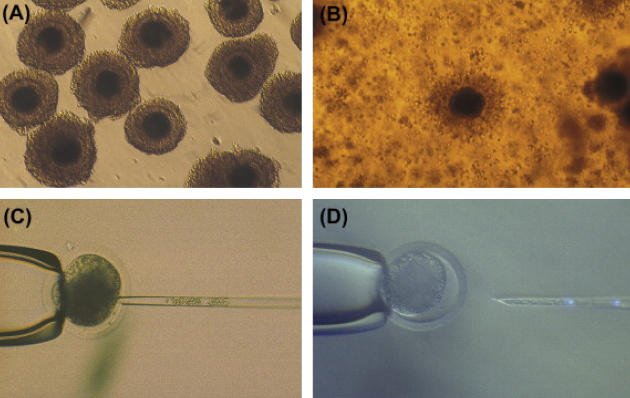
Но как именно ооцит меняет ядро зрелой соматической клетки, было неизвестно до работ Яманаки — он разобрался, что запускает этот процесс, и повторил его на зрелом фибробласте. В 2012 году ученый получил за это Нобелевскую премию, которую разделил с британским биологом Джоном Гердоном, впервые использовавшим SCNT на лягушках в конце 1950-х. В 2008 году iPSC получили из человеческих кератиноцитов — поверхностных клеток кожи, в 2010 — из клеток крови, а потом и из некоторых других.
Для превращения зрелой клетки в iPSC требуются особые белки — факторы транскрипции, которые переносят инструкции к участкам ДНК, где расположены нужные гены. Так можно активировать те из них, что отключены в зрелой клетке, то есть «эмбриональные», и выключить те, что делают ее специализированной. А чтобы в клетке стали синтезироваться нужные факторы транскрипции, в нее сначала должны попасть гены, кодирующие их. Команде Яманаки удалось перепрограммировать фибробласты, используя всего четыре таких гена — их и кодируемые ими факторы транскрипции теперь называют факторами Яманаки.
Сначала для доставки в клетку нужных генов использовали вирусные векторы , но так в ее генетический материал попадали лишние фрагменты. Поэтому ученые разработали и другие способы. Например, плазмиды можно вводить в клетку с помощью электрического разряда, создающего временное отверстие в клеточной мембране.
Но в настоящее время возможна и «вирусная» доставка, так как появились технологии, мешающие интеграции внешнего генетического материала в геном клетки. Также в качестве вектора научились использовать аденовирус, который не встраивает свои гены в геном хозяина, в отличие от тех, что применяли раньше.

Факторы Яманаки — самая стандартная комбинация для получения iPSC. Но любой из них можно заменить — например, родственным фактором транскрипции или малыми молекулами , имитирующими их работу. Сейчас ученые пробуют использовать разные «коктейли».
Готовые iPSC могут сколько угодно долго делиться в лаборатории. Когда нужно превратить их в специализированную клетку, ученые изменяют условия среды или внедряют в клетку «активаторы» генов, заставляющих ее созреть нужным образом. За годы экспериментов они разработали некоторые базовые «рецепты» для правильной специализации плюрипотентных клеток в нужные типы.
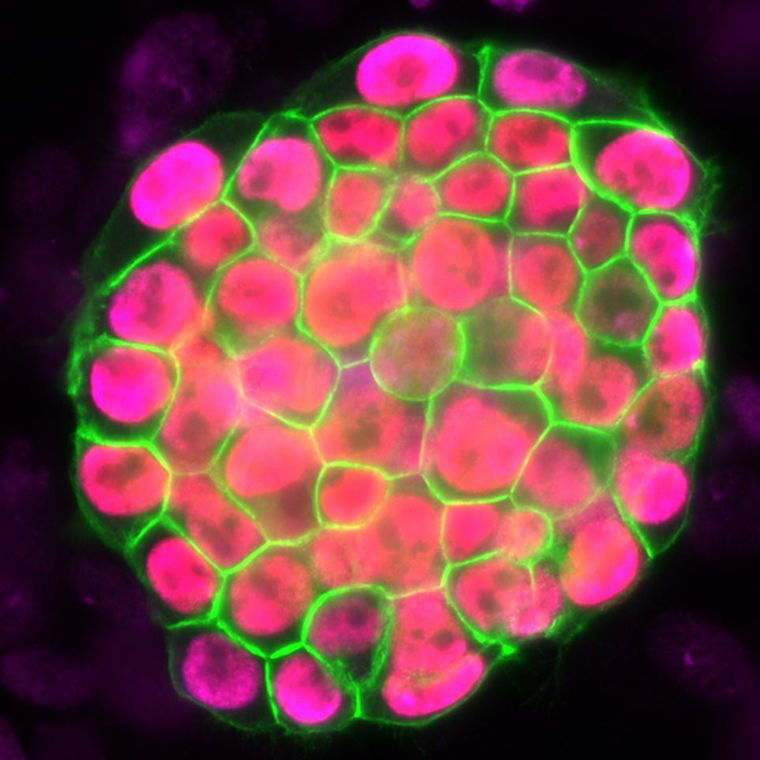
Зачем ученым нужны такие новые клетки
Для научных исследований. Некоторые клетки, например кожи, крови или клетки опухолей, можно легко получить от живых доноров. Но клетки сердца или нейроны в «живом» виде ученым практически недоступны.
Например, механизмы развития нейродегенеративных болезней ранее можно было изучать только на животных моделях или с помощью посмертного анализа тканей мозга. А теперь можно «готовить» нейроны из iSPC и следить за их развитием. В том числе ученые пробуют получать нервные клетки напрямую из клеток кожи, минуя незрелую стадию. Это помогает сохранить признаки старения и делает их ближе к клеткам тех, кто страдает от возрастных болезней вроде Альцгеймера и Паркинсона.
Еще iPSC можно получить из клеток людей, страдающих разными заболеваниями, — они будут нести мутации, вызывающие болезнь, или генетические факторы риска. Это полезно для моделирования целого ряда заболеваний, в основном наследственных, например семейной болезни Альцгеймера .
Нейроны, полученные из таких iPSC, будут воспроизводить признаки нужного состояния. Например, в них будет накапливаться токсичный белок бета-амилоид, как и в нервных клетках человека, заболевшего упомянутой формой наследственной деменции.
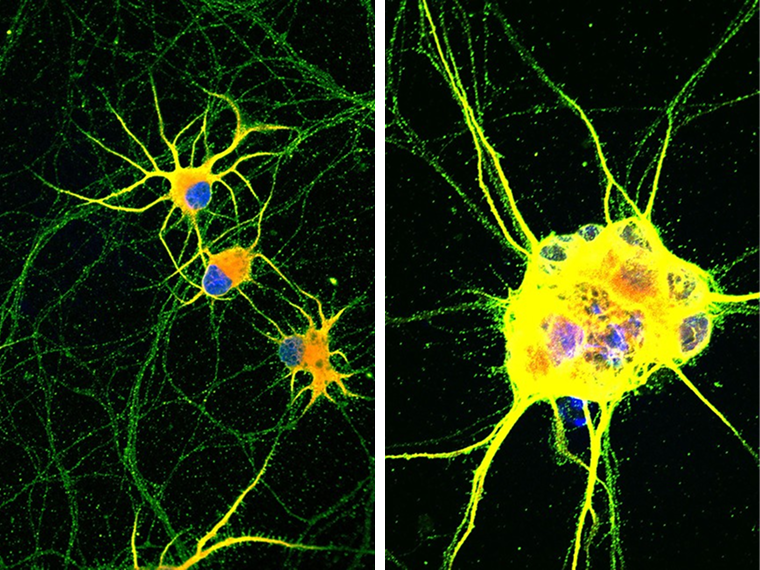
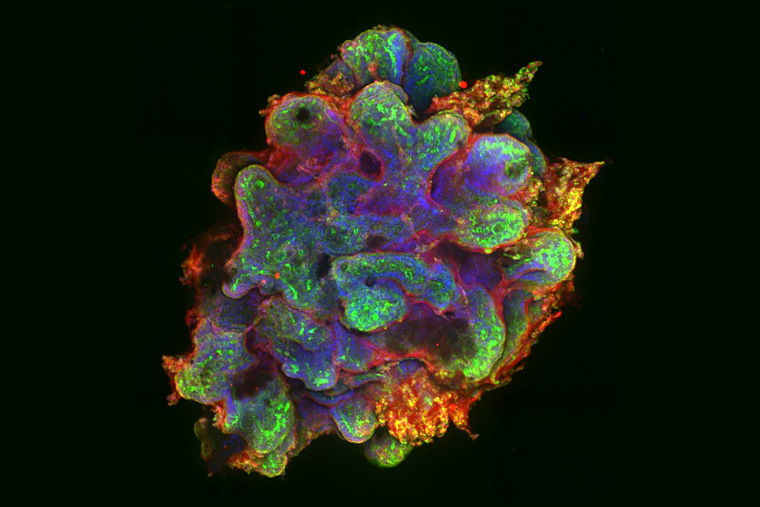
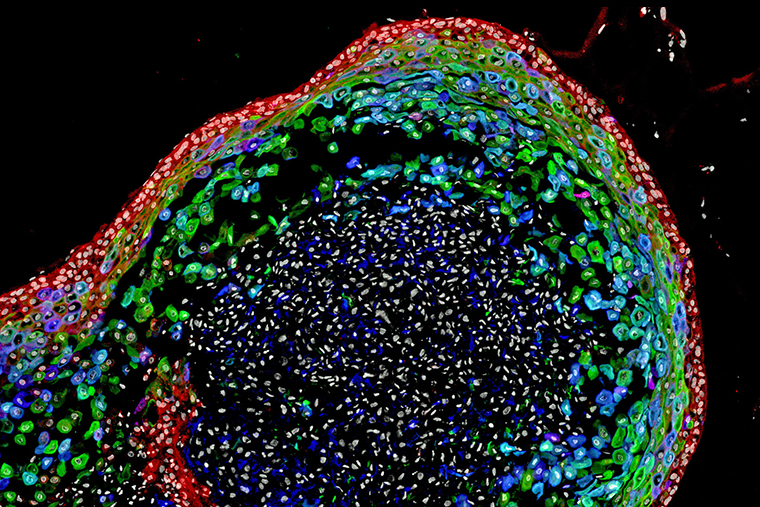
Иногда iPSC выращивают в двумерной культуральной чашке, как на уроках биологии. Иногда — в трехмерной среде, где они могут расти и в высоту, а не только одним плоским слоем, это называют 3D-культурой клеток. Так можно добиться образования многоклеточных кластеров — органоидов, напоминающих участки сложных органов, таких как мозг и почки. Сейчас ученые научились достигать впечатляющей сложности органоидов, хотя, конечно, до настоящих органов в этом плане им еще далеко. Но они уже могут состоять из разных типов тканей и представляют собой более реалистичные модели для исследователей.
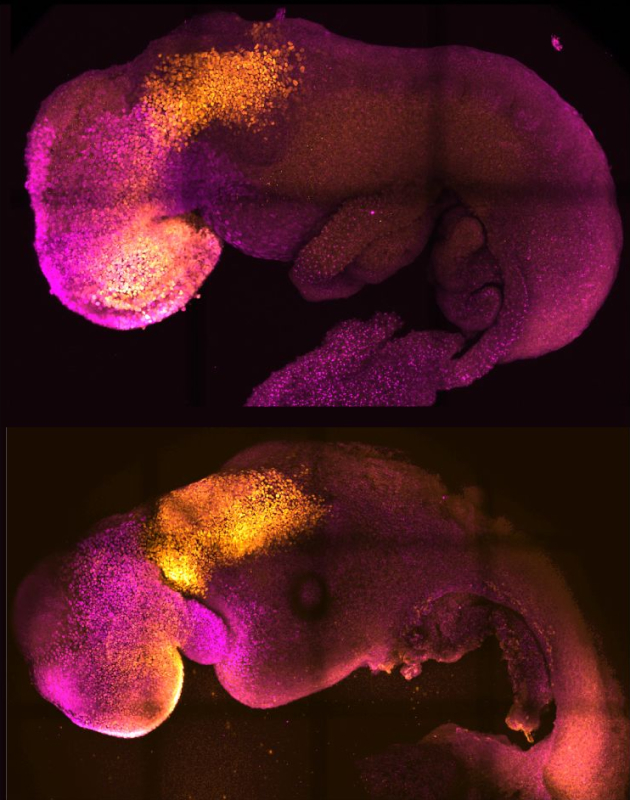
Также ученые использовали iPSC для создания структур, напоминающих человеческий эмбрион. Это, например, позволило изучить события первых десяти дней его развития, еще до имплантации в стенку матки. Кроме того, клетки, полученные из iPSC, помогают разрабатывать лекарственные препараты, в частности проверять их токсичность.
Для лечения болезней и трансплантации органов. В перспективе iPSC можно будет использовать для терапии самых разных заболеваний и травм, например повреждений спинного мозга, подсаживая новые нейроны взамен разрушенных.
Так, уже проходят клинические испытания лечения диабета первого типа с помощью iPSC. При этом заболевании у человека не работает участок поджелудочной железы, который вырабатывает инсулин . Ученые вырастили нужные клетки органа из собственных жировых клеток женщины, болеющей диабетом первого типа, и пересадили ей под мышцы живота. В итоге с болезнью удалось справиться: участница исследования перестала зависеть от инъекций инсулина через три месяца.
Взять уже готовые клетки поджелудочной железы у донора тоже можно — и так делают. Но после пересадки донорских тканей человеку придется всю жизнь принимать лекарства, подавляющие иммунитет. Это нужно, чтобы избежать уничтожения чужеродных клеток иммунной системой. А на собственные модифицированные клетки организм реагировать не будет, и никакой терапии после их подсадки не понадобится.
В перспективе с помощью iPSC можно будет создавать целые органы для трансплантации. Пока это еще невозможно, так как они состоят из сложного набора тканей, пронизанных кровеносными сосудами и нервами. Заставить плюрипотентные стволовые клетки повторить все виды тканей и выполнять нужные функции еще не получается. Но ученые работают в этом направлении.
Например, в начале 2000-х они вырастили мышечные и эпителиальные клетки мочевого пузыря, а потом засеяли ими специальный каркас. Полученный органоид использовали, чтобы восстановить мочевой пузырь у семи человек с тяжелыми пороками развития.
При использовании iPSC у людей есть ряд сложностей. Основная — важно следить, чтобы в процессе перепрограммирования не произошло мутаций, из-за которых клетка впоследствии превратится в раковую и даст начало опухоли в теле человека. Также из образца клеток для трансплантации должны быть удалены все недифференцированные iPSC: они тоже склонны к перерождению в злокачественные.
Кроме того, есть сложности с введением и приживлением таких клеток, особенно в нервной системе. Поэтому клеточная терапия с использованием iPSC еще находится на начальной стадии развития.
А что с яйцеклетками?
Ученые также пытаются создать функционирующие половые клетки, или гаметы, в частности женские ооциты, из обычных клеток, чтобы люди с бесплодием могли завести генетически родных детей. Технологию получения таких клеток называют гаметогенезом in vitro, то есть в пробирке.
Получать гаметы пытаются разными способами, но сделать это сложнее, чем вырастить новые клетки тела. Например, не получится просто так создать половые клетки из iPSC. Дело в том, что в гаметах не 46 хромосом, как в соматических клетках, а 23, половинный набор, — как минимум надо добиться исчезновения лишней половины. Также незрелые клетки должны приобрести другие особенности половых клеток. Например, в цитоплазме ооцитов должны быть специальные факторы, нужные, чтобы одна клетка могла дать начало целому организму.
Поэтому iPSC сначала пытаются превратить в ранних предшественников половых клеток, а потом помогают созревать. В организме людей этот сложный процесс проходит в несколько стадий и в случае яйцеклеток длится около 10 лет, что создает ученым дополнительные сложности. При этом работающие гаметы у мышей так получать уже удавалось. У человека же этот процесс сопряжен со множеством технических препятствий.

Для упрощения ученые пытаются модифицировать технологию клонирования. В ядре клетки кожи, которое в этом случае помещают в ооцит, полный набор хромосом, то есть 46. Как мы уже знаем, если оставить все как есть, разовьется организм, генетически идентичный женщине, у которой взяли соматическую клетку. Но нужно получить ребенка с комбинацией генов от мамы и папы.
Эта задача решается так: забирают ядро у клетки кожи, остановленной на одной из начальных стадий деления. Его помещают в женскую половую клетку донора, из которой предварительно извлекли ядро, а потом вводят внутрь нее сперматозоид. После ряда некоторых хитрых манипуляций ядро клетки кожи теряет лишнюю половину хромосом и сливается с ядром сперматозоида — почти как при обычном оплодотворении. Затем оплодотворенная клетка делится, давая начало эмбриону с генами обоих родителей.
Именно этот механизм и реализовали ученые в сентябре 2025 года. Правда, не все тестовые ооциты дошли до итоговой стадии зрелой яйцеклетки и оплодотворения, а в тех случаях, когда они смогли это сделать, не всегда получались нормальные эмбрионы. Число хромосом, близкое к нужному, получилось примерно в 20% случаев. То есть технология еще далека до клинического применения у людей.
Что в итоге
Стволовые клетки можно взять в готовом виде, например из эмбриональных тканей человека. Но это связано с этическими сложностями, кроме того, такого материала для исследований всегда не хватает. Поэтому ученые научились создавать стволовые клетки из того, что легко получить, например из образцов кожи. Из них потом можно вырастить почти любые клетки человеческого тела, чтобы изучать с их помощью действие лекарств и моделировать развитие заболеваний.
У вас тоже есть каверзный медицинский вопрос? Задайте его нам, и мы попробуем найти ответ!