Белки-убийцы: что такое прионы и можно ли защититься от прионных болезней
Прионами называют белки, которые могут вести себя как инфекционные агенты, например вирусы.
Иногда ими можно заразиться, но в большинстве случаев они возникают случайно в главном органе человеческого тела — мозге. А стоит только одной такой устойчивой молекуле появиться внутри нервной клетки, как она заставляет превращаться в прионы другие, еще нормальные белки. Потом этот процесс распространяется от нейрона к нейрону — и мозг перестает работать как нужно, а человек сталкивается с симптомами, напоминающими деменцию.
Расскажем подробнее, что такое прионы, какие болезни они вызывают и можно ли их предотвратить.
Что такое прионы и как они вызывают болезни
Прионы — неправильно свернутые белки, которые действуют на своих нормальных соседей того же вида так, что они тоже меняют форму. Потом эти неправильные молекулы слипаются, образуя длинные белковые нити — фибриллы. А это нарушает работу клетки.
Все классические прионные заболевания связаны с мисфолдингом, то есть неправильным сворачиванием, белка PrP, которого особенно много в мозге. PrP способен принимать множество аномальных форм — их называют штаммами. У каждого свои свойства, и они связаны с разными болезнями, которые объединяют в общую группу и называют губчатыми, или спонгиоформными, энцефалопатиями.
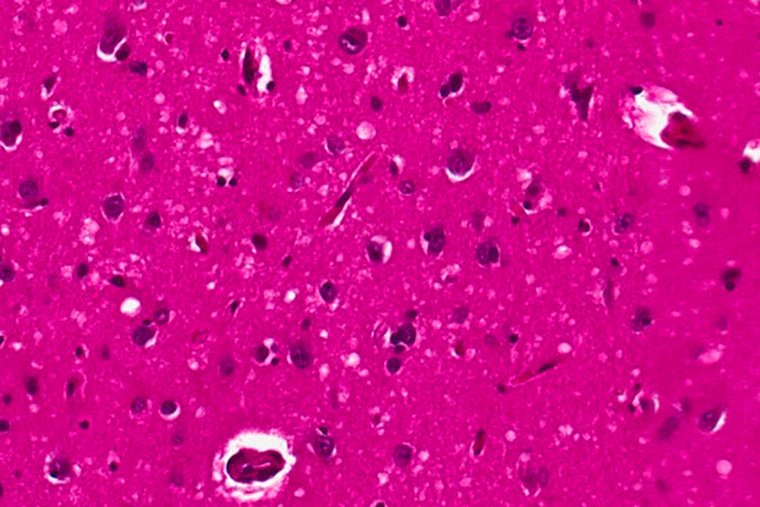
Такое название появилось из-за того, что ткани мозга человека или животного, умершего от прионного заболевания, под микроскопом в буквальном смысле выглядят как губка: целые группы нейронов умирают, оставляя в органе множественные крошечные полости.
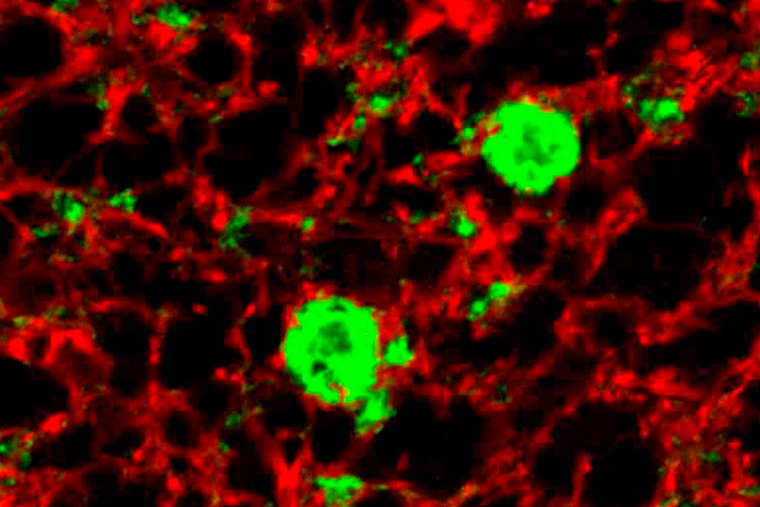
При этом PrP — не единственный белок, способный быть прионом. Сейчас считается, что развитие многих нейродегенеративных болезней также связано с аномальными белками — в том числе Альцгеймера и Паркинсона, бокового амиотрофического склероза и лобно-височной деменции . Так, при болезни Альцгеймера в мозге образуются и распространяются неправильные формы белков бета-амилоида и тау, а при болезни Паркинсона — альфа-синуклеина.
Прионоподобные белки ответственны не только за болезни нервной системы — они могут поражать и другие органы. Самый известный пример — АА-амилоидоз, при котором в почках и печени откладывается аномальный амилоид. Это состояние развивается у людей с хроническими инфекциями и воспалениями: туберкулезом, болезнью Крона, ревматоидным артритом. Также есть данные, что при сахарном диабете второго типа за гибель клеток поджелудочной железы, производящих инсулин, частично может отвечать неправильно свернутый островковый амилоидный полипептид (IAPP).
Как ученые обнаружили прионы
Началом истории прионов считают 1950-е годы, когда американский вирусолог Карлтон Гайдузек и медицинский работник Винсент Зигас описали куру — смертельное неврологическое заболевание, которым страдали люди племени форе на севере Папуа — Новой Гвинеи. Название болезни переводится как «дрожь»: сильный тремор тела был одним из симптомов заболевания. Люди с куру постепенно теряли контроль над движениями и неизбежно умирали.
В 1976 году Гайдузек получил Нобелевскую премию за свое открытие: он понял, что это инфекционная болезнь, передающаяся из-за традиций каннибализма. В племени было принято готовить и поедать умерших родственников. Причем чаще всего болели женщины и дети, которым по традиции доставался мозг погибших. Инкубационный период состояния был долгим: могло пройти от 5 до 50 лет с момента заражения до первых симптомов.


Позже американский врач Стенли Прузинер открыл, что причина куру и других болезней с похожими симптомами — прионы. За это он тоже получил Нобелевскую премию в 1997 году.
Сама идея о том, что белки могут вызывать заболевания, тогда была сенсационной и вызывала много споров. Значительная часть ученых считала, что возбудители — вирусы, просто их никак не получается обнаружить. Но Прузинеру удалось получить препарат из мозга зараженных хомяков, который содержал только один инфекционный агент — неправильный белок. Все эксперименты указывали на то, что именно он вызывает заболевание. Прузинер и назвал его прионом — это сокращение от infectious protein, инфекционный белок.
Позже также было доказано, что прионный белок может инициировать цепную реакцию, в результате которой нормальный PrP превращается в более стабильную зловредную форму. Причем она чрезвычайно устойчива: сохраняется при температурах свыше 100 °C и после обработки органическими растворителями. Со временем инфекционная форма белка накапливается в мозге, что повреждает нейроны и вызывает симптомы болезни.
Прузинер вместе с другими учеными выделил прионный ген PrP и показал, что этот белок — обычный компонент многих тканей организма. Также он доказал, что прионные болезни не только могут передаваться, но и бывают генетическими — вызванными мутациями в гене приона. Для этого ученые вывели мышей с мутантными генами — все они заболели энцефалопатией. А если у грызунов, наоборот, подавляли ген приона, они становились устойчивыми к заражению и не заболевали после введения в мозг аномальных белков. При этом восприимчивость к инфекции возвращалась после того, как функцию гена восстанавливали.
Интересно, что мыши, у которых прионный ген не работал, в остальном были здоровы. Из-за этого ученые предположили, что нормальный PrP им не очень и нужен. До сих пор роль этого белка остается загадкой: никто не понимает, какие функции он выполняет и почему его так много в нервной системе. Например, есть гипотезы, что он участвует в механизмах памяти и регуляции продолжительности жизни клеток, но как это работает, до конца непонятно.

Какие прионные болезни чаще всего встречаются и можно ли ими заразиться
Все губчатые энцефалопатии называют трансмиссивными, то есть передающимися, так как аномальный белок способен заражать своей неправильной формой соседей (сайт недоступен из РФ). При этом далеко не все эти болезни можно отнести к по-настоящему заразным.
Например, губчатыми энцефалопатиями болеют многие животные: овцы, верблюды, коровы, кошки, олени. Но в большинстве случаев прионы не способны преодолеть межвидовой барьер. Например, скрепи овец известна несколько веков, но случаев ее передачи людям не зафиксировано. Но от коров, больных коровьим бешенством, люди могут заразиться, съев загрязненное прионами мясо. После этого разовьется одна из форм болезни Крейтцфельдта — Якоба, или БКЯ. При этом возникают спутанность сознания, нарушения координации и другие неврологические симптомы.
Вспышка такого заболевания была зафиксирована в Великобритании и ряде других стран в 1990-х годах из-за того, что в корм крупному рогатому скоту добавляли переработанные части трупов умерших и забитых животных, в частности мясокостную муку. Коровы начали болеть коровьим бешенством, но их мясо считалось безопасным для людей, пока у тех не начали диагностировать БКЯ. В итоге ввели строгий ветконтроль над этим заболеванием, а также изменили правила кормления жвачных животных. После этого коровье бешенство было практически искоренено, а употребление говядины считается безопасным.
В середине 20 века в Северной Америке впервые выявили губчатую энцефалопатию у оленей — ее назвали хронической изнуряющей болезнью. С тех пор случаи зарегистрированы в половине штатов США, Канаде, Норвегии, Финляндии и некоторых других странах. Пока точно неизвестно, может ли она передаваться человеку, но теоретически это вероятно — например, при употреблении заболевших животных в пищу. Так, была описана ситуация, когда два охотника из одной группы, которые ели мясо оленей, заболели БКЯ.
От человека при обычном контакте заразиться прионной болезнью нельзя: для этого надо тесно проконтактировать с его головным или спинным мозгом либо получить прионы внутрь, например съесть, как было с куру в Папуа — Новой Гвинее. В 1970—1980-х годах десятки человек заразились БКЯ после трансплантации твердой мозговой оболочки, инъекций человеческого гормона роста, полученного из мозга умерших людей, и операций по пересадке роговицы.
В настоящее время для профилактики таких случаев человеческий мозг не используют при производстве препаратов или трансплантатов — например, препараты гормона роста теперь синтезируют в лаборатории. С 1974 года роговицу глаз для пересадки не забирают у людей с неврологическими болезнями или умерших по неизвестным причинам.
Меры по профилактике передачи прионных заболеваний привели к тому, что сейчас встречаются только единичные случаи заражения ими через еду, из-за переливания крови и загрязненных нейрохирургических инструментов — менее 1% от всех случаев инфекции. Учитывая, что губчатые энцефалопатии в целом встречаются редко, вероятность ими заразиться куда меньше, чем выиграть в лотерею.
Еще 10—15% случаев таких заболеваний вызваны наследственными генетическими мутациями. Например, фатальная семейная бессонница: в среднем в возрасте около 50 лет люди с ней начинают плохо спать, у них развиваются многочисленные неврологические и когнитивные нарушения. Примерно через полтора года наступает смерть.
Другой пример: болезнь Герстмана — Штраусслера — Шейнкера, наследственная деменция, симптомы обычно появляются до 50—60 лет, от начала болезни до смерти в среднем проходит 3—4 года. Болезнь Крейтцфельдта — Якоба тоже может быть наследственной, тогда ее называют семейной.

Наследственные прионные заболевания нельзя предотвратить, но можно предсказать их по генетическому анализу, если такие случаи были в семье. Человек, у которого обнаружена опасная мутация, полученная от родителей, рано или поздно заболеет. Сдавать такие тесты всем не нужно: эти заболевания редки, поэтому тестирование назначают только близким родственникам заболевших.
Например, сейчас известно менее чем о 10 семьях с фатальной семейной бессонницей во всем мире. В 2013 году впервые выявлена наследственная прионная болезнь, поражающая не только центральную, но и периферическую нервную систему, — она встречается всего в двух семьях. Первые симптомы этого заболевания не связаны с нарушениями работы мозга: в 20—30 лет у людей появляется сильная диарея, нарушается чувствительность конечностей, может быть задержка или недержание мочи. А к 50—60 годам добавляются когнитивные нарушения.
Но около 90% прионных заболеваний связаны со спонтанным неправильным сворачиванием нормального белка — предсказать их не получится. Такие случаи называют спорадическими. Они возникают из-за случайных мутаций, когда в клетках начинает образовываться патологический белок, или случайного изменения формы PrP уже после образования. Точная причина этого неизвестна, и как предотвратить превращение нормального белка в прион — тоже неясно.
Разные трансмиссивные губчатые энцефалопатии проявляются по-разному, поскольку прионы могут принимать уникальные формы с различными биохимическими свойствами и сначала поражают разные части мозга. Различия есть даже при разных формах одной болезни. Например, при спорадической БКЯ вместе с другими симптомами возникают нарушения памяти, а при варианте этой болезни, передающемся от коров, — психиатрические нарушения, такие как сильная тревога и депрессия. При этом все прионные болезни заканчиваются распространением неправильно свернутых белков, разрушением мозга и смертью.
У человека прионные заболевания встречаются редко — пара случаев на миллион, в основном болеют люди старше 60 лет. Так, в США фиксируют около 500 случаев каждый год, подавляющее большинство из них, 450 случаев, — спорадическая болезнь Крейтцфельдта — Якоба.
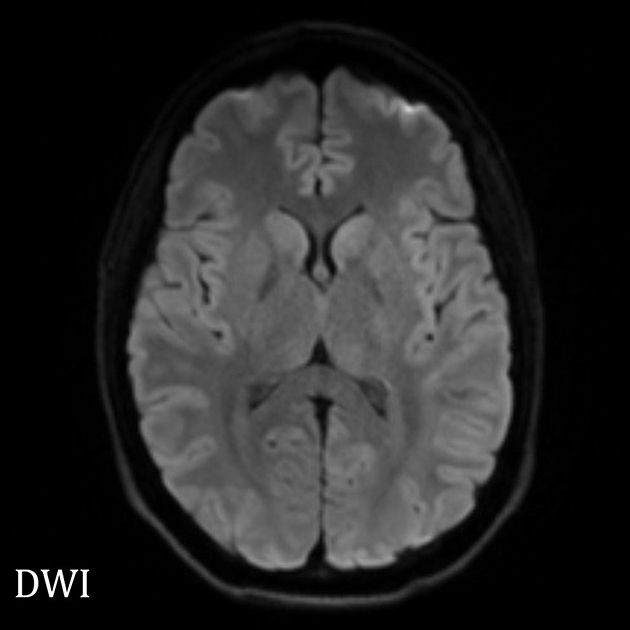
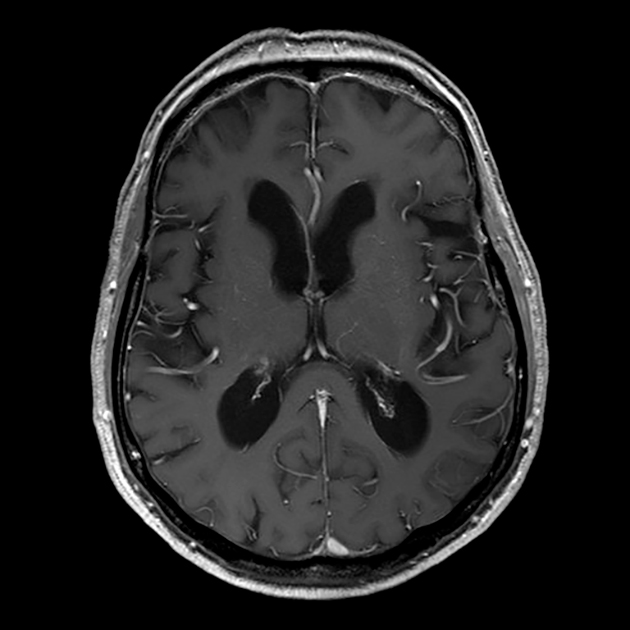
В России точной статистики нет, что связано в том числе со сложностью постановки диагноза, в частности с отсутствием современных тестов, находящих прионы в биологических жидкостях. Без них болезнь можно заподозрить по изменениям на МРТ головного мозга, но зачастую точно установить, что у человека была прионная инфекция, можно только посмертно. В список особо опасных заболеваний, о которых больницы должны уведомлять Роспотребнадзор, губчатые энцефалопатии не входят.
Можно ли вылечить прионные болезни
Нет. Если у человека появились симптомы, вылечить его невозможно — показана только паллиативная помощь . Ученые пытаются разработать методы терапии, но это сложно, в частности из-за механизма развития прионных болезней, при которых нужно «починить» мелкие молекулярные поломки в головном мозге. Такая же история и со многими заболеваниями, связанными с прионоподобными белками, например с болезнью Альцгеймера. Ее исследуют больше, так как она встречается чаще, но до сих пор нет работающего средства остановить или хотя бы замедлить разрушение мозга.
Помочь справиться с наследственными прионными болезнями может генная терапия, но пока такие методы опробованы только на животных. Также фармкомпании начинают исследовать антисмысловые олигонуклеотиды — фрагменты синтетической ДНК, которые вводят в спинномозговую жидкость. Затем они разрушают матричную РНК клеток, нужную для производства белков, впоследствии сворачивающихся в прионы.
Кроме того, исследователи пытаются разработать малые молекулы или антитела , действующие на более поздних стадиях процесса. Например, предотвращающие неправильное сворачивание PrP или уменьшающие повреждения, вызванные его патогенными формами. Но пока все эти методы терапии на стадии разработки.
У вас тоже есть каверзный медицинский вопрос? Задайте его нам — и мы попробуем найти ответ!